从超声炮首证,看“械三证”竞争下的医美江湖

行业竞争加剧。
今年,不论是头部美妆企业、医美机构还是医药巨头、电商平台,都在加码医美领域。C2CC传媒X新妆也围绕医美市场发布多篇文章:
随着医美产业链发展加速,国内医美市场迎来火热扩张,上游产业的国产品牌加速替代国际大牌。据《2025医美行业白皮书》数据显示,我国医美市场规模已逼近3700亿元,2020-2025年间年均增速保持17.4% 的高位。预计2030年,整体市场规模有望突破7000亿元,未来五年年均增速预计达13.2%。
近日,深圳半岛医疗集团股份有限公司(以下简称:半岛医疗)旗下的聚焦超声皮肤治疗仪(商品名:半岛大超炮)正式获得了国家药监局颁发的三级医疗器械认证,成为全球首款且目前唯一获国家药监局批准上市的三类超声医美设备。
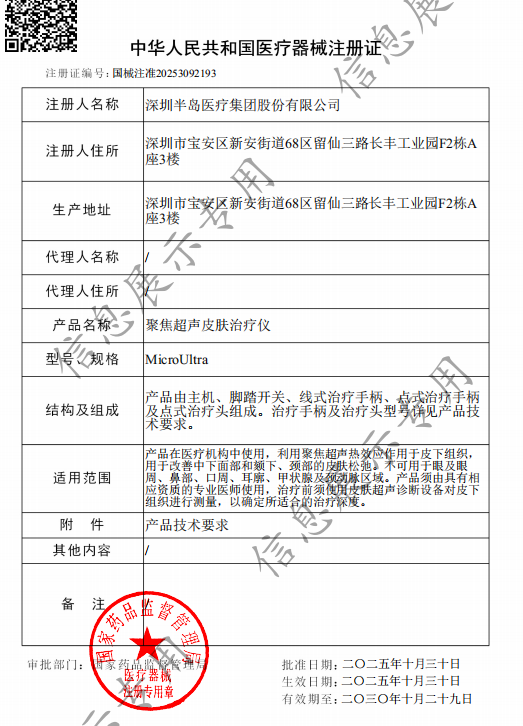
这张证书不仅是产品上市通行证,更是国产医美设备打破高端医美设备长期被进口品牌主导,迈入高阶合规时代的重要标志。
01
超声炮“鼻祖”半岛医疗
拿下行业首张“械三证”
公开资料显示,半岛医疗成立于2008年,是集研产销为一体的国家级专精特新“小巨人”企业,十余年来深耕光电研发及皮肤治疗领域。公司总部和研发中心位于深圳,在华南、华中与西南等地设有数处生产与运营中心,已获得FDA、CE、NMPA等近70余项全球认证,获授权专利500余项,累计为1万余家医院和医疗机构提供优质的服务和设备,累计销售仪器10万余台。
公司主营整形美容、皮肤治疗与产康/私密康复三大业务板块,核心产品大致可分为以“黄金微针/黄金微雕/黄金射频/黄金私密”等为核心的微针与射频系列、以“半岛超声炮/超声治疗仪”为代表的超声类治疗设备、以及“半岛白极光(皮秒 Nd:YAG)”“高频点雕”“舒敏治疗仪”“腋臭治疗系统”“308 光疗仪”等皮肤治疗与家用系列机型。
其最为人熟知的,还是超声炮系列产品。
2021年6月,半岛医疗“超声治疗仪”获国家药监局颁发的第二类医疗器械注册证,成为国内首个获得NMPA认证的超声类医疗设备,而“超声炮”这个更易传播的别称正是由半岛医疗提出并为人熟知。
经半岛医疗统计,自2021年推出半岛超声炮后,截至2024年年底,累计治疗人次已超过400万,相当于平均每天有超过3000人接受该项治疗。
此次获得械三证的“半岛大超炮”,实则为半岛超声炮的3.0版本。

据官方介绍,半岛大超炮将原有的“单发模式”升级为“TEET影子发射模式”,大幅提升产品的治疗密度;搭载的“AI能控系统”与“舒感脉冲技术”,能够避免表皮热损伤与神经刺激。还首次配置了“智能超声影像系统”,是目前市面上作用层次最深的无创抗衰设备,能精准针对皮肤各层次衰老问题。
但需注意的是,产品仅适用于改善中下面部、下巴和颈部的皮肤松弛,而鱼尾纹、法令纹、眼袋等皮肤问题所涉及眼周、鼻部、口周、耳廓、甲状腺及颈动脉区域都在禁用之列。
02
企业竞争加剧
打响“械三证”争夺战
国内医疗器械依据风险程度由低到高,可分为第一类、第二类、第三类,其中,“械三证”因其技术壁垒高、市场独占性强,已成为企业发展的核心竞争力力。
一方面,拿下械三证意味着其产品在安全性和有效性上已达到最高标准,并在合规性上占据了先发优势;另一方面,械三证能在市场观望情绪浓厚的前提下,直接转化为消费者信任与购买决策,成为品牌破局关键。
因此,即便“械三证”是国家药监局对高风险医疗器械产品的严格准入证明,审批流程复杂且研发投入巨大,仍然有大批医美企业争相申报。目前,根据技术赛道和市场特点,目前国内的医美设备“械三证”市场可以大致划分为注射类、射频类、超声医美类几大板块。
美容仪所在的频射类赛道,自2022年被纳入Ⅲ类医疗器械管理后,彻底进入分水岭。由于技术门槛高,合规资质已成为品牌进入头部阵营的关键门槛,未获批品牌在缓冲期内面临清退。
其中,半岛医疗自主研发的“半岛逆时针”射频皮肤治疗仪获得国产射频微针领域首张械三证,美容仪品牌雅萌在今年6月拿下械三证,成为首个射频Ⅲ类获证国际美容仪品牌。雅萌护肤闪修仪PRO在吴千语直播中GMV达348W+,成为当场直播当中的Top2销售品牌。
与射频类面临同样境遇的超声医美,也于2023年11月被划入第三类医疗器械管理。在监管部门对医美超声设备加强规范管理下,多个厂家的超声治疗仪产品在注册适用范围中去掉了“用于医疗机构康复科、皮肤科、整形美容科”等表述。在此背景下,半岛大超炮获得首张超声医美三类证对行业影响深远。
相比之下,注射类赛道竞争则更为激烈。
锦波生物作为医美黑马,自2021年起独揽国内仅有的三张重组胶原蛋白医美械三证,其核心产品“薇旖美”销量突破200万支,带领公司实现四年营收增超6倍,净利增近13倍,5年连续双位数增长的亮眼成绩。更是在今年6月,吸引前首富钟睒睒通过旗下养生堂有限公司斥资34亿元战略入股。(相关阅读:连续5年双位数暴涨!“医美黑马”14亿业绩和新“风暴” 丨 鲜锋)
而这一垄断格局现已被巨子生物打破。10月21日,巨子生物旗下“重组I型α1亚型胶原蛋白冻干纤维”获批业内第四张重组胶原蛋白"械三证"。此外,巨子生物和创健医疗还有多款胶原蛋白植入剂产品获受理,敷尔佳、福瑞达等企业也在布局相关产品。

华熙生物在4月连获两张械三证后,截至5月共拥有 13 项三类医疗器械批文。其中, 11 项为医美注射类产品,这一数据远超爱美客(8 项)、昊海生物(4 项)、艾尔建(9 项)、锦波生物(3项)等企业,稳居行业首位。
9月1日,大连富勒烯药业有限公司旗下的“注射用透明质酸钠溶液”正式获批上市,成为国内第六款合规的三类医疗器械水光针产品。
从医美材料角度分析,重组胶原蛋白是企业申报“拿证”的大热领域,玻尿酸竞争也已进入白热化阶段。据国家药监局数据显示,截至2024年年底,境内医疗器械“胶原蛋白”注册、获批产品超过800个。2024年,玻尿酸三类医疗器械产品获批数量超过70个,许多企业通过同一注册证推出多规格产品的“一证多品”策略降低成本,树立价格优势。
不难看出,现阶段企业对“械三证”的竞争已从单一产品审批升级为技术储备、资本运作与政策适应力的多维较量。
03
合规化时代
医美行业迎来又一轮洗牌
2024年-2025年7月,共有43款三类械注射类产品、2款注射用A型肉毒素产品、22款三类械光电类医美治疗产品获药监局批准上市,3款针对肥胖或超重适应症的注射类产品获批。
对已有械三证的企业来说,他们不仅享受合规红利窗口期,还拥有更长的品牌建设周期,先发优势明显。但随着同类型产品持续获批上市,如何通过技术储备、多元布局、成分协同实现产品和功效的差异化战略,将成为企业脱颖而出的关键。
尤其是,中国医美器械行业即将步入一个更聚焦合规发展与技术创新的新阶段。
11月4日,国家药品监督管理局发布新版《医疗器械生产质量管理规范》(2025年第107号公告),这一重磅文件将于2026年11月1日正式实施,取代已运行十年的2014年版规范。
对比旧版,新版《规范》首次明确医疗器械注册人、备案人对产品质量安全承担主体责任,即使委托生产,责任也不转移。这与旧规仅强调“生产企业”负责形成鲜明对比。
也对关键岗位人员的提供了明确的准入标准,且资质要求得到大幅提升。例如,管理者代表要求具备二类、三类医疗器械企业要求本科及以上学历或中级职称,质量部门负责人同样需满足相应学历和工作经验要求,企业负责人、管理者代表等关键岗位人员必须为全职人员。
同时,新版《规范》明确要求将风险管理贯穿设计开发、生产、销售和售后服务全过程,强调定期实施质量风险管理回顾;新增了旧规中没有的“鼓励企业推进数智化转型,提高生产和质量管理效能”全新理念;并对信息化系统、电子记录、数据完整性的有了详细要求,顺应数字化转型趋势。
政策收紧与合规化浪潮在短期内可能带来行业阵痛,但长远来看,这为真正具备创新能力的企业扫清了“劣币驱逐良币”的障碍。医美行业将从以往的“营销驱动”转向“产品驱动”和“技术驱动”,半岛医疗等一批深耕技术研发的企业,也会借此机会持续不断的进行产品和技术创新,推动国产医美设备走向世界舞台。
免责声明
本网刊发或转载各类资讯,是出于传递更多信息之目的,并不以赢利为目的,也不意味着赞同其观点或证实其内容的真实性。
C2CC历来重视版权等知识产权保护,如本网转载之部分资讯、稿件涉及版权等问题,请作者在本网发布该文两周内速来电或来函与我们联系,C2CC会及时处理。
凡本网原创稿件,版权归本网所有,并遵循CC创作共用约定。其他媒体(包括网络媒体和传统媒体)转载C2CC原创稿件时须在明显位置注明信息来源:C2CC中国化妆品网。


